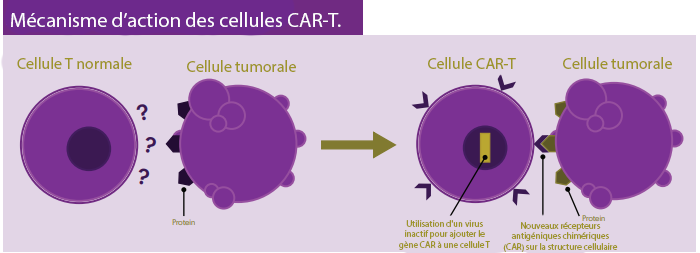
À qui s’adresse le traitement par CAR T-cell?
La CAR-T traite actuellement certains sous-types agressifs de lymphomes. En plus du sous-type et du stade, les médecins devront également évaluer l’état de santé général du patient, sa forme physique et les circonstances entourant la thérapie, ce qui peut comprendre les comorbidités du patient, sa capacité à supporter un traitement intensif ainsi que sa volonté et sa capacité à se déplacer pour le traitement.
Il existe des critères d’admissibilité particuliers pour chaque thérapie CAR T-cell, qui reposent sur les enseignements issus d’essais cliniques et d’approbations réglementaires.
De façon générale, la thérapie par CAR T-cell est indiquée pour les patients suivants, soit ceux :
- ayant reçu un diagnostic d’un sous-type de lymphome, et pour qui on a approuvé la thérapie CAR T-cell;
- répondant aux critères réglementaires (ex. : deux rechutes et traitements antérieurs);
- dont la tumeur exprime l’antigène spécifique ciblé par la thérapie;
- dont la fonction de l’organe et le niveau de performance sont satisfaisants;
- ne présentant aucune infection active;
- n’ayant pas d’importantes dysfonctions sur le plan des systèmes immunitaire, neurologique ou cardiaque
Les médecins discuteront de l’admissibilité de ces patients et enverront les dossiers médicaux pertinents au centre spécialisé en soins oncologiques. Le centre qui administre la thérapie CAR T-cell devra faire l’objet d’une évaluation pour le traitement.
Efficacité clinique
Il est important de comprendre les résultats obtenus à la suite d’un traitement par thérapie CAR T-cell, car si les premiers résultats sont positifs chez certains patients, l’efficacité clinique varie considérablement d’un patient à l’autre. Le candidat idéal fait encore l’objet d’essais cliniques. Certains patients obtiennent une rémission à long terme. Mais actuellement, la thérapie CAR T-cell n’est pas encore considérée comme un moyen de guérison, car des données supplémentaires seront nécessaires pour déterminer si les patients qui obtiennent une rémission complète demeurent exempts de la maladie à long terme.
Les résultats mesurés obtenus dans le cadre des essais cliniques sont les suivants :
Taux de réponse complète (RC)
Le pourcentage de patients qui répondent au traitement avec la disparition de tous les signes du cancer. Même si les patients n’obtiennent pas de RC, ils peuvent présenter une réponse partielle (RP). Le taux de réponse globale est la somme de la RC et de la RP.
Survie médiane globale (SMG)
Durée médiane durant laquelle les patients sont encore en vie à compter de la date du diagnostic ou du début du traitement.
Survie sans progression (SSP)
La durée pendant et après le traitement durant laquelle un patient vit avec la maladie sans que celle-ci ne progresse ou ne s’aggrave.
Effets secondaires
La thérapie CAR T-cell entraîne plusieurs effets secondaires à court et à long terme. On conseille aux patients de rester près de leur centre de traitement durant quelques semaines. La plupart des effets secondaires à court terme peuvent être gérés à l’aide de thérapies de soutien. Cependant, d’autres effets secondaires peuvent être plus graves et potentiellement mortels ainsi que nécessiter un traitement dans l’unité de soins intensifs de l’hôpital.
Syndrome de libération de cytokines
Lorsque les cellules CAR-T sont libérées et qu’elles se multiplient dans l’organisme du patient, son système immunitaire est fortement activé et libère un nombre massif de cytokines inflammatoires dans le sang, provoquant ainsi le syndrome de libération de cytokines (SLC). Cela peut se produire au cours de la première semaine suivant la perfusion ou plus tard dans certains cas.
La durée et l’intensité du SLC peuvent varier. Certains patients ne présentent que de légers symptômes pseudo-grippaux, tandis que d’autres souffrent de fortes fièvres, d’hypoxie (déficit en oxygène), de tension artérielle basse ou de toxicité dans de nombreux organes.
Neurotoxicité (désormais désigné syndrome de neurotoxicité associé aux cellules immunitaires effectrices ou CIE ou encore en anglais ICANS, soit Immune effector cell-associated neurotoxicity symdrome)
Le CIE désigne les cellules effectrices du système immunitaire. Les cellules CAR-T peuvent avoir un effet sur le cerveau du patient, susceptible de causer chez lui un état de confusion, d’agitation et une perte de conscience. Les patients peuvent souffrir de maux de tête, de difficultés à s’exprimer par écrit ou oralement, d’anxiété et de crises d’épilepsie occasionnelles.
La neurotoxicité peut se produire avec ou sans syndrome de libération de cytokines. Si un patient présente également un SLC, les symptômes neurologiques apparaissent plus fréquemment après la présence du syndrome. Dans la plupart des cas, ils sont réversibles, mais dans de rares cas, un œdème cérébral associé à la neurotoxicité peut se développer, ce qui est potentiellement fatal.
Syndrome d’activation macrophagique
Inflammation grave du système immunitaire, pouvant entraîner une défaillance de plusieurs organes.
Neutropénie fébrile
Diminution anormale du nombre de certains globules blancs dans le sang, associée à de la fièvre.
Aplasie des cellules B
Faible nombre de cellules B ou absence de cellules B.
Anémie
Nombre de globules rouges inférieur à la normale.
Thrombocytopénie
Diminution du nombre de plaquettes dans le sang.
Hypogammaglobulinémie
Réduction de tous les types de gamma-globulines, y compris les anticorps qui aident à combattre les infections.
Les effets secondaires graves sont souvent le résultat de l’activité élevée du système immunitaire induite par la thérapie CAR T-cell. On utilise des médicaments immunosuppresseurs et des corticostéroïdes dans la gestion des symptômes dans le but de réduire les effets secondaires sans éliminer complètement les cellules CAR-T.
Il est important que les patients et les soignants puissent identifier rapidement les symptômes afin qu’ils soient traités de manière appropriée, d’autant plus que certains effets secondaires (comme la neurotoxicité) sont les mêmes que ceux d’autres pathologies que l’on traite très différemment.
Comment avoir accès à la thérapie CART-cell et quels en sont les défis actuels?